국내 세포 조사결과 15일 나올 예정이우석 대표 “식약처에 적극 협조”식약처, 모든 가능성 열고 철저검증
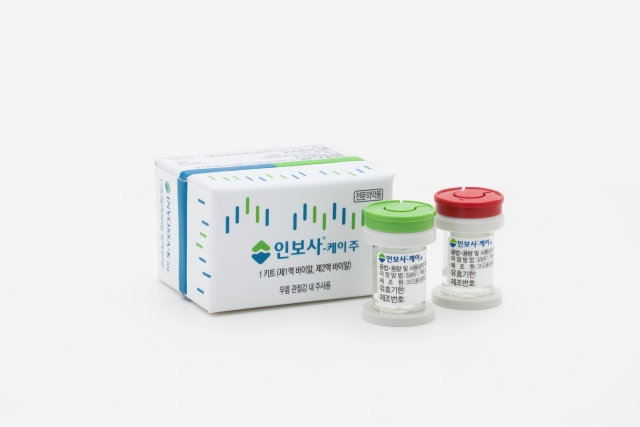
인보사는 사람 연골세포(HC)와 연골세포 성장인자((TGF-β1)를 도입한 형질전환세포)를 3대1로 섞어 무릎 관절강에 주사하는 형태로, 주로 중등도 무릎 골관절염 치료에 쓰인다.
현재 인보사는 미국 임상 3상 진행 중 주성분 중 하나인 형질전환세포(TC)가 허가를 받았던 연골유래세포가 아닌 293세포(신장세포)인 것이 확인되면서 지난달 31일부터 국내유통 및 판매가 중지된 상황이다. 코오롱생명과학 측은 국내에서 유통되는 인보사에도 신장유래세포가 포함됐는지를 미국 업체에 분석의뢰했고 이 결과가 15일 발표될 예정이다.
가장 가능성이 높은 시나리오는 국내 상용화된 인보사에서도 신장유래세포가 확인되는 것 이다. 코오롱생명과학은 동일한 세포주를 배양해 한국과 미국이 각각 나눠 가져 국내 시판 인보사도 신장유래세포로 확인될 가능성이 매우 높고 해당 물질로 임상시험 등을 거쳐 안전성과 유효성을 입증했으니 허가 취소 대상은 아닐 것이라고 기대하고 있다.
하지만 회사측의 바람대로 단순히 허가변경으로 끝날 사안은 아니라는 것이 업계의 중론이다. 일단 신장유래세포의 혼입 원인을 명확하게 확인해야한다.
식약처는 코오롱생명과학과는 별개로 자체검증을 위해 코오롱생명과학에 인보사의 세포를 요청한 상태다. 코오롱생명과학은 인보사를 제조하는 충주공장에 있는 세포를 식약처에 넘겼으며 미국의 세포는 국내 반입절차를 진행중이다. 또한 현재 충주공장에 대한 실사에 들어갔으며 15일 조사결과가 나온 이후에도 자체적인 조사를 진행할 예정이다.
최악의 시나리오는 식약처 조사에서 세포 혼입 과정에서의 고의성이나 자료조작으로 의심되는 부분이 발견되거나 미국에서 확인된 신장유래세포가 국내에서는 확인되지 않는 것이다.
만약 이러한 결과로 허가취소 처분이 내려진다면 파장은 일파만파 커지게 된다. 안전성은 물론이며 개발의 모든 과정을 신뢰할 수 없게 되기 때문이다.
이우석 코오롱생명과학 대표는 “허가 변경으로 결론낼 수 있도록 과학적으로 식약처를 최대한 설득할 것”이라며 ”식약처의 모든 요구에 적극적으로 응하겠다”고 말했다.

뉴스웨이 이한울 기자
han22@newsway.co.kr
<저작권자 © 온라인 경제미디어 뉴스웨이 · 무단 전재 및 재배포 금지>





















댓글